Hromna kiselina
 | |
| Nazivi | |
|---|---|
| IUPAC naziv Hromna kiselina | |
| Sistemski IUPAC naziv Dihidroksidodioksidohromijum | |
| Drugi nazivi Hromna(VI) kiselina Tetraoksohromna kiselina | |
| Identifikacija | |
| |
3D model (Jmol) |
|
| ChEBI |
|
| ChemSpider |
|
| ECHA InfoCard | 100.028.910 |
| EC broj | 231-801-5 |
| Gmelin Referenca | 25982 |
| |
SMILES
| |
| Svojstva | |
| CrH2O4 | |
| Molarna masa | 118,01 g·mol−1 |
| Agregatno stanje | crveni kristali |
| Gustina | 1,201 g cm-3 |
| Tačka topljenja | 197 °C (387 °F; 470 K) |
| Tačka ključanja | 250 °C (482 °F; 523 K) |
Rastvorljivost u vodi | 1666.6 g dm-3 |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
 Y verifikuj (šta je Y verifikuj (šta je  Y Y Н ?) Н ?) | |
| Reference infokutije | |
Hromna kiselina je smeša formirana dodavanjem koncentrovane sumporne kiseline u dihromat. Ona može da sadrži više jedinjenja, među kojima je hrom trioksid. Ova vrsta hromne kiseline se može koristiti kao smeša za čišćenje stakla. Hromna kiselina takođe može da bude molekul H2CrO4 kome je trioksid anhidrid. Hromna kiselina sadrži hrom u oksidacionom stanju +6 (ili VI). Ona je jak i korozivan oksidacioni agens.[3][4]
Molekulska hromna kiselina
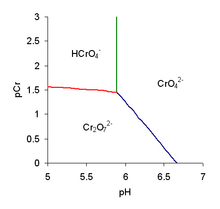
Molekulska hromna kiselina, H2CrO4, je slična sumpornoj kiselini, H2SO4. Obe su klasifikovane kao jake kiseline, mada se samo njihov prvi proton lako gubi.
- H2CrO4 ⇌ [HCrO4]− + H+
pKa ravnoteže nije dobro karakterisana. Objavljene vrednosti variraju između −0.8 do 1.6.[5] Vrednost na jonskoj jačini nula je teško odrediti zato što se polu disocijacija jedino javlja u veoma jako kiselim rastvorima, na oko pH nula, i.e koncentracija kiseline je oko 1 mol dm−3. Dodatni problem je da jon [HCrO4]− ima tendenciju da se dimerizuje, uz gubitak molekula vode, čime se formira dihromatni jon, [Cr2O7]2−:
- 2 [HCrO4]− ⇌ [Cr2O7]2− + H2O, log KD = 2.05.
Dihromat se može protonisati[6]:
- [HCr2O7]− ⇌ [Cr2O7]2− + H+, pK = 1.8
pK vrednost ove reakcije pokazuje da se to može ignorisati na pH > 4.
Do gubitka drugog protona dolazi u pH opsegu 4-8, te je jon [HCrO4]− slaba kiselina.
Molekulska hromna kiselina se u principu može formirati dodatkom hrom trioksida u vodu (slično proizvodnji sumporne kiseline).
- CrO3 + H2O ⇌ H2CrO4
međutim u praksi dolazi do reverzibilne reakcije pri čemu se hromna kiselina dehidratiše. Do toga dolazi kad se koncentrovana sumporna kiselina doda u rastvor dihromata. Prvo se boja promeni iz narandžaste (dihromat) do crvene (hromna kiselina) i zatim bordo kristali hrom trioksida precipitiraju iz smeše, bez dalje promene boje. Boje su posledica promena kompleksa prenosa naboja.
Hrom trioksid je anhidrid molekulske hromne kiseline. On je Luisova kiselina te može da reaguje sa Luisovim bazama, kao što je piridin u nevodenoj sredini, poput dihlorometana (Kolinsov reagens).
Dihromna kiselina
Dihromna kiselina, H2Cr2O7, je potpuno protonisani dihromatni jon. Ona je proizvod dodavanja hrom trioksida u molekulsku hromnu kiselinu.
- [Cr2O7]2− + 2H+ ⇌ H2Cr2O7 ⇌ H2CrO4 + CrO3
Reference
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003. уреди
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3. изд.). Prentice Hall. ISBN 978-0-13-175553-6.
- ^ Holleman A. F.; Wiberg E. (2001). Inorganic Chemistry (1st изд.). San Diego: Academic Press. ISBN 0-12-352651-5.
- ^ IUPAC SC-Database Архивирано на сајту Wayback Machine (19. јун 2017) A comprehensive database of published data on equilibrium constants of metal complexes and ligands
- ^ Brito, F.; Ascanioa, J.; et al. (1997). „Equilibria of chromate(VI) species in acid medium and ab initio studies of these species”. Polyhedron. 16 (21): 3835—3846. doi:10.1016/S0277-5387(97)00128-9.
Spoljašnje veze
- Интернационална карта хемијске безбедности 1194
- Hrom i hromna jedinjenja











