Isobutan
| Isobutan | |
|---|---|
 Strukturní vzorec isobutanu | |
 3D model isobutanu | |
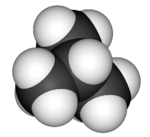 3D model isobutanu | |
| Obecné | |
| Systematický název | 2-methylpropan |
| Triviální název | isobutan |
| Ostatní názvy | izobutan, iso-butan, izo-butan, methylpropan |
| Anglický název | Isobutane |
| Německý název | Isobutan |
| Sumární vzorec | C4H10 |
| Vzhled | bezbarvý plyn |
| Identifikace | |
| Registrační číslo CAS | 75-28-5 |
| EC-no (EINECS/ELINCS/NLP) | 200-857-2 |
| Indexové číslo | 601-004-00-0 |
| SMILES | CC(C)C |
| Vlastnosti | |
| Molární hmotnost | 58,123 g/mol |
| Teplota tání | −159,6 °C |
| Teplota varu | −11,7 °C |
| Hustota | 2,51 kg/m3 (plyn, 15 °C) 593,4 kg/m3 (kapalina, -11,7 °C) |
| Dynamický viskozitní koeficient | 0,006 89 cP (0 °C) |
| Kritická teplota Tk | 134,9 °C |
| Kritický tlak pk | 369 5 kPa |
| Rozpustnost ve vodě | 3,25 % objemově (20 °C) |
| Bezpečnost | |
 GHS02  GHS04 Nebezpečí[1] | |
| H-věty | H220 |
| R-věty | R12 |
| S-věty | (S2) S9 S16 |
| NFPA 704 |  4 1 |
| Teplota vznícení | 460 °C |
| Meze výbušnosti | 1,8 - 8,4 % |
Některá data mohou pocházet z datové položky. | |
Isobutan (též izobutan; systematický název methylpropan nebo 2-methylpropan) je alkan izomerní s butanem. Obavy z poškozování ozónové vrstvy freony vedly ke zvýšenému používání isobutanu jako chladiva, zvláště v chladničkách a mrazničkách pro domácnosti, a jako hnacího plynu ve sprejích. Pro tato použití se označuje jako R-600a. Některé tábornické vařiče využívají směs isobutanu s propanem, obvykle 80:20. Isobutan se používá i jako surovina v petrochemickém průmyslu, například pro syntézu isooktanu[2]. Isobutan je R-skupina v aminokyselině leucinu.
Názvosloví
Isobutan je triviální název podporovaný IUPAC v Doporučení pro názvosloví organické chemie 1993[3]; aktuálně je již nedoporučovaný.
Systematický název je methylpropan. Číslo substituentu (2-) není potřeba uvádět, protože neexistuje izomer této molekuly, který by měl „methylpropan“ jako součást názvu. Dle nejnovějšího IUPAC názvosloví (2013) však je v preferovaném názvu potřeba lokant uvádět (methyl posunutý do polohy 1 tvoří jinou sloučeninu; že už nejde o methylpropan, ale butan, nehraje roli).
Reference
V tomto článku byl použit překlad textu z článku Isobutane na anglické Wikipedii.
- ↑ a b Isobutane. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ Patent Watch, July 31, 2006.. www.chemistry.org [online]. [cit. 2009-08-18]. Dostupné v archivu pořízeném dne 2007-03-11.
- ↑ Panico, R.; & Powell, W. H. (Eds.). A Guide to IUPAC Nomenclature of Organic Compounds 1993. Oxford: Blackwell Science, 1994. ISBN 0-632-03488-2. http://www.acdlabs.com/iupac/nomenclature/93/r93_679.htm
Externí odkazy
 Obrázky, zvuky či videa k tématu Isobutan na Wikimedia Commons
Obrázky, zvuky či videa k tématu Isobutan na Wikimedia Commons - International Chemical Safety Card 0901
- NIOSH Pocket Guide to Chemical Hazards
- IUPAC Nomenclature of Organic Chemistry Archivováno 8. 6. 2011 na Wayback Machine. (online version of the "Blue Book")
- Data from Air Liquide[nedostupný zdroj]
 | Tento článek je příliš stručný nebo postrádá důležité informace. Pomozte Wikipedii tím, že jej vhodně rozšíříte. Nevkládejte však bez oprávnění cizí texty. |
| Chladiva | |
|---|---|
| CFC a další halogenderiváty | R-10 (tetrachlormethan) • R-11 (trichlorfluormethan) • R-12 (dichlordifluormethan) • R-12B1 (bromchlordifluormethan) • R-12B2 (dibromdifluormethan) • R-13 (chlortrifluormethan) • R-13B1 (bromtrifluormethan) • R-14 (tetrafluormethan) • R-20 (trichlormethan (chloroform)) • R-21 (dichlorfluormethan) • R-22 (chlordifluormethan) • R-22B1 (bromdifluormethan) • R-23 (trifluormethan (fluoroform)) • R-30 (dichlormethan) • R-31 (chlorfluormethan) • R-32 (difluormethan) • R-40 (chlormethan) • R-41 (fluormethan) • R-125 (pentafluorethan) • R-130 (1,1,2,2-tetrachlorethan) • R-130a (1,1,1,2-tetrachlorethan) • R-134a (1,1,1,2-tetrafluorethan) • R-150 (1,2-dichlorethan) • R-160 (chlorethan) • R-218 (oktafluorpropan) • R-1120 (trichlorethylen) |
| Uhlovodíky | |
| Ostatní látky | R-610 (diethylether) • R-611 (methylformiát) • R-630 (methylamin) • R-631 (ethylamin) • R-702 (vodík) • R-704 (helium) • R-717 (amoniak) • R-718 (voda) • R-720 (neon) • R-728 (dusík) • R-732 (kyslík) • R-740 (argon) • R-744 (oxid uhličitý) • R-744a (oxid dusný) • R-7640 (oxid siřičitý) • R-784 (krypton) |









